
- লেখক Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:34.
- সর্বশেষ পরিবর্তিত 2025-01-22 16:56.
সাধারণভাবে উদ্ধৃত খুঁজে পেতে আয়নকরণ শক্তি , এই মান a-এর পরমাণুর সংখ্যা দ্বারা গুণিত হয় আঁচিল হাইড্রোজেন পরমাণুর (অ্যাভোগাড্রো ধ্রুবক) এবং তারপর রূপান্তর করতে 1000 দ্বারা ভাগ করা জুলস প্রতি কিলোজুল . এটি হাইড্রোজেনের জন্য সাধারণত উদ্ধৃত মানের সাথে তুলনা করে আয়নকরণ শক্তি 1312 এর kJ mol -1.
এখানে, আপনি কিভাবে be3+ এর আয়নায়ন শক্তি খুঁজে পাবেন?
দ্য আয়নকরণ শক্তি এটি Z^2 এর সমানুপাতিক, যেহেতু এটি পরমাণু/আয়নের স্থল অবস্থা এবং এর মধ্যে পার্থক্য শক্তি বিচ্ছিন্ন আয়ন প্লাস ইলেকট্রনের। Be^(4+) এর চার্জ H^+ এর চারগুণ, তাই আয়নকরণ শক্তি Be^(3+) এর 4^2 বা H এর 16 গুণ।
একইভাবে, আয়নিকরণ শক্তি কিসের জন্য ব্যবহৃত হয়? আয়নকরণ শক্তি গুরুত্বপূর্ণ কারণ এটি হতে পারে অভ্যস্ত রাসায়নিক বন্ধনের শক্তি ভবিষ্যদ্বাণী সাহায্য. ইউনিট: আয়নকরণ শক্তি প্রতি মোল (kJ/mol) বা ইলেক্ট্রন ভোল্ট (eV) এককে কিলোজুল রিপোর্ট করা হয়।
পরবর্তীকালে, কেউ জিজ্ঞাসা করতে পারে, আপনি কীভাবে আয়নকরণের সম্ভাব্যতা গণনা করবেন?
আয়নিত হওয়া ভরকে পারমাণবিক ভর সংখ্যা দিয়ে গ্রামে ভাগ করুন। আপনার যদি 24 গ্রাম অক্সিজেন থাকে, উদাহরণস্বরূপ, যার পারমাণবিক ভর 16, আপনার 1.5 মোল আছে। গুণ করুন আয়নকরণ শক্তি আপনি 96.485 দ্বারা দেখছেন. 1 eV/কণা 96.485 kJ/mol এর সমান।
আয়নিকরণ শক্তি উদাহরণ কি?
দ্য আয়নকরণ শক্তি একটি পরমাণুর পরিমাণ হল শক্তি সেই পরমাণু বা আয়নের বায়বীয় রূপ থেকে একটি ইলেকট্রন অপসারণ করতে হবে। 1সেন্ট আয়নকরণ শক্তি - দ্য শক্তি সর্বোচ্চ অপসারণ প্রয়োজন শক্তি একটি নিরপেক্ষ গ্যাসীয় পরমাণু থেকে ইলেকট্রন। জন্য উদাহরণ : না(g) → না+(g) + ই- আমি1 = 496 kJ/mol.
প্রস্তাবিত:
আপনি কিভাবে একটি ইলেক্ট্রোম্যাগনেটিক তরঙ্গের শক্তি গণনা করবেন?

যেকোনো তরঙ্গ দ্বারা বাহিত শক্তি তার প্রশস্ততা বর্গক্ষেত্রের সমানুপাতিক। ইলেক্ট্রোম্যাগনেটিক তরঙ্গের জন্য, এর অর্থ হল তীব্রতাকে Iave=cϵ0E202 I ave = c ϵ 0 E 0 2 2 হিসাবে প্রকাশ করা যেতে পারে, যেখানে Iave হল W/m2-এ গড় তীব্রতা এবং E0 হল একটানা সাইনোসয়েডাল তরঙ্গের সর্বাধিক বৈদ্যুতিক ক্ষেত্রের শক্তি।
আপনি কিভাবে জল দ্বারা তাপ শক্তি গণনা করবেন?

তাপের গণনা করার পরে, আপনি Q = mc ∆T, অর্থাৎ Q = (100 + 100) x4.18 x 8 ব্যবহার করেন। জলের নির্দিষ্ট তাপ ক্ষমতাকে 4181 জুলস/কেজি ডিগ্রি সেলসিয়াস 1000 দ্বারা ভাগ করে জুল/জি ডিগ্রির চিত্র পেতে C. উত্তর হল 6,688, যার মানে হল 6688 জুল তাপ নির্গত হয়
আপনি কিভাবে শক্তি তীব্রতা এবং দূরত্ব গণনা করবেন?

যেহেতু তীব্রতা হল প্রতি ইউনিট ক্ষেত্রফলের শক্তি, আপনি যদি উৎসের শক্তিকে গোলকের ক্ষেত্রফল দিয়ে ভাগ করেন, তাহলে আপনি উৎস থেকে r দূরত্বে তীব্রতা গণনা করবেন। এই সূত্রটি স্থানান্তর করা আপনাকে উত্সের শক্তি গণনা করতে সক্ষম করে: P = 4πr2I
আপনি কিভাবে প্রকৃত শক্তি এবং আপাত ক্ষমতা গণনা করবেন?
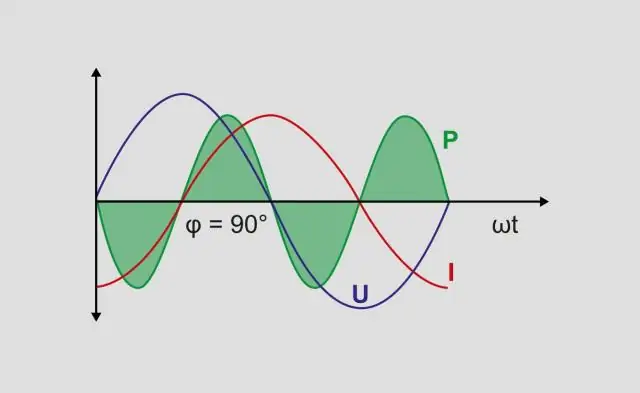
প্রতিক্রিয়াশীল শক্তি এবং সত্যিকারের শক্তির সংমিশ্রণকে আপাত শক্তি বলা হয় এবং এটি একটি সার্কিটের ভোল্টেজ এবং কারেন্টের গুণফল, ফেজ এঙ্গেলের রেফারেন্স ছাড়াই। আপাত শক্তি ভোল্ট-অ্যাম্পস (VA) এর এককে পরিমাপ করা হয় এবং বড় অক্ষর S দ্বারা প্রতীকী হয়
আপনি কিভাবে শক্তি তীব্রতা গণনা করবেন?

মহাকাশের একটি বিন্দুতে শক্তির ঘনত্ব (একক আয়তনে শক্তি) নিয়ে এবং শক্তিটি যে গতিতে চলছে তার দ্বারা এটিকে গুণ করে তীব্রতা পাওয়া যায়। ফলস্বরূপ ভেক্টরে ক্ষেত্রফল দ্বারা বিভক্ত শক্তির একক রয়েছে (যেমন, পৃষ্ঠের শক্তি ঘনত্ব)
