
সুচিপত্র:
- লেখক Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:34.
- সর্বশেষ পরিবর্তিত 2025-01-22 16:56.
দ্য সংখ্যা এর বন্ড একটি নিরপেক্ষ পরমাণুর জন্য সমান সংখ্যা সম্পূর্ণ ভ্যালেন্স শেলের ইলেকট্রন (2 বা 8 ইলেকট্রন) বিয়োগ সংখ্যা ভ্যালেন্স ইলেকট্রন এর। এই পদ্ধতি কাজ করে কারণ প্রতিটি সমযোজী বন্ধন যে একটি পরমাণু গঠন তার চার্জ পরিবর্তন না করে একটি পরমাণুর ভ্যালেন্স শেলে আরেকটি ইলেকট্রন যোগ করে।
সহজভাবে, কোন যৌগটি সমযোজী বন্ধন ধারণ করে?
উদাহরন স্বরুপ যৌগ যে ধারণ কেবল সমযোজী বন্ধনের মিথেন (CH4), কার্বন মনোক্সাইড (CO), এবং আয়োডিন মনোব্রোমাইড (IBr)। সমযোজী বন্ধন হাইড্রোজেন পরমাণুর মধ্যে: যেহেতু প্রতিটি হাইড্রোজেন পরমাণুতে একটি করে ইলেকট্রন থাকে, তাই তারা একজোড়া ইলেকট্রন ভাগ করে তাদের বাইরের খোলস পূরণ করতে সক্ষম হয় সমযোজী বন্ধন.
কেউ জিজ্ঞাসা করতে পারে, একটি পরমাণু কয়টি সমযোজী বন্ধন গঠন করতে পারে? একটি হাইড্রোজেন পরমাণু 1টি বন্ধন গঠন করতে পারে, একটি কার্বন পরমাণু গঠন করতে পারে 4 বন্ধন, একটি নাইট্রোজেন পরমাণু 3টি বন্ধন গঠন করতে পারে এবং একটি অক্সিজেন পরমাণু 2টি বন্ধন গঠন করতে পারে। চলুন প্রশ্ন বিরতি. প্রথমত সমযোজী বন্ধন হল ভ্যালেন্স ইলেকট্রন এবং নিউক্লিয়াসের ভাগ করা জোড়ার মধ্যে আকর্ষণের শক্তিশালী ইলেক্ট্রোস্ট্যাটিক শক্তি।
এটি বিবেচনা করে, সমযোজী বন্ধনের 5টি উদাহরণ কী?
কোভ্যালেন্ট বন্ডের উদাহরণ:
- জল. একটি উদাহরণ জল। জল একটি সমযোজী বন্ধন নিয়ে গঠিত যা হাইড্রোজেন এবং অক্সিজেন বন্ধন যুক্ত করে H তৈরি করে2ও.
- হীরা। একটি হীরা কার্বনের দৈত্য সমযোজী বন্ধনের উদাহরণ। একটি হীরার একটি বিশাল আণবিক গঠন রয়েছে।
- Vulcanized রাবার. আরেকটি উদাহরণ হল ভলকানাইজড রাবার।
3 ধরনের সমযোজী বন্ধন কি কি?
দ্য তিন প্রকার অন্যান্য উত্তরে উল্লিখিত পোলার সমযোজী , অপোলার সমযোজী , এবং সমন্বয় সমযোজী . প্রথম, পোলার সমযোজী , দুটি অধাতুর মধ্যে গঠিত হয় যার তড়িৎ ঋণাত্মকতার পার্থক্য রয়েছে। তারা তাদের ইলেকট্রন ঘনত্ব অসমভাবে ভাগ করে নেয়।
প্রস্তাবিত:
আপনি কিভাবে একটি রাসায়নিক সূত্রে অণুর সংখ্যা খুঁজে পাবেন?
অ্যাভোগাড্রো ধ্রুবক দ্বারা মোলগুলিকে গুণ করুন আপনার নমুনায় অণুর সংখ্যা গণনা করতে অ্যাভোগাড্রো ধ্রুবক, 6.022 x 10^23 দ্বারা মোলের সংখ্যাকে গুণ করুন
আপনি কিভাবে পরীক্ষামূলকভাবে একটি যৌগ আয়নিক বা সমযোজী কিনা তা নির্ধারণ করতে পারেন?

একটি বন্ধন আয়নিক বা সমযোজী কিনা তা নির্ধারণ করার জন্য কয়েকটি ভিন্ন উপায় রয়েছে। সংজ্ঞা অনুসারে, একটি আয়নিক বন্ধন একটি ধাতু এবং একটি অধাতুর মধ্যে এবং একটি সমযোজী বন্ধন 2টি অধাতুর মধ্যে। সুতরাং আপনি সাধারণত পর্যায় সারণীটি দেখেন এবং নির্ধারণ করেন যে আপনার যৌগটি একটি ধাতু/অধাতু দিয়ে তৈরি নাকি মাত্র 2টি অধাতু।
আপনি কিভাবে একটি গ্রাফে দুটি বিন্দুর মধ্যে দূরত্ব খুঁজে পাবেন?
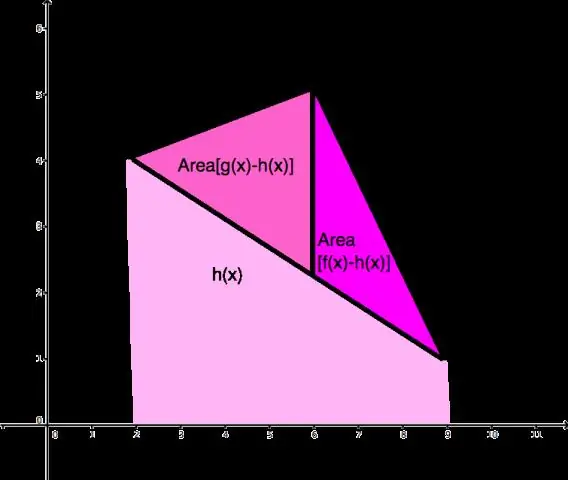
ধাপ দুটি বিন্দুর স্থানাঙ্ক নিন যা আপনি দূরত্ব খুঁজে পেতে চান। একটি পয়েন্ট পয়েন্ট 1 (x1,y1) কল করুন এবং অন্য পয়েন্ট 2 (x2,y2) করুন। দূরত্ব সূত্র জানুন। পয়েন্টগুলির মধ্যে অনুভূমিক এবং উল্লম্ব দূরত্ব খুঁজুন। উভয় মানকে বর্গ করুন। বর্গাকার মান একসাথে যোগ করুন। সমীকরণের বর্গমূল নিন
আপনি কিভাবে একটি সিরিজের পরবর্তী সংখ্যা খুঁজে পাবেন?

প্রথমত, অনুক্রমের জন্য সাধারণ পার্থক্য খুঁজুন। দ্বিতীয় পদ থেকে প্রথম পদ বিয়োগ করুন। তৃতীয় পদ থেকে দ্বিতীয় পদ বিয়োগ করুন। পরবর্তী মান খুঁজে পেতে, শেষ প্রদত্ত সংখ্যা যোগ করুন
আপনি কিভাবে একটি সংখ্যা লাইনের যোগফল খুঁজে পাবেন?

যোগফল বের করতে একটি সংখ্যা রেখা ব্যবহার করুন egin{align*}4 + (ext{-}6)end{align*}। প্রথমে আপনার নাম্বারলাইন আঁকুন। তারপর, সংখ্যা লাইনে 4 (আপনার যোগফলের প্রথম পূর্ণসংখ্যা) এর অবস্থান খুঁজুন। এর পরে, লক্ষ্য করুন যে এই সেকেন্ড পূর্ণসংখ্যা, -6, ঋণাত্মক
