
- লেখক Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:34.
- সর্বশেষ পরিবর্তিত 2025-01-22 16:56.
দ্য চার কোয়ান্টাম সংখ্যা বর্ণনা করতে ব্যবহৃত ইলেকট্রন হল n=2, ℓ=1, m=1, 0, বা -1, এবং s=1/2 (the ইলেকট্রন সমান্তরাল স্পিন আছে)।
অধিকন্তু, চারটি কোয়ান্টাম সংখ্যা একটি ইলেকট্রন সম্পর্কে কী বর্ণনা করে?
সম্পূর্ণরূপে বর্ণনা একটি ইলেকট্রন একটি পরমাণুতে, চার কোয়ান্টাম সংখ্যা প্রয়োজন: শক্তি (n), কৌণিক ভরবেগ (ℓ), চৌম্বকীয় মোমেন্ট (mℓ), এবং স্পিন (মিs) প্রথম কোয়ান্টাম সংখ্যা বর্ণনা করে দ্য ইলেকট্রন শেল, বা শক্তির স্তর, একটি পরমাণুর।
একইভাবে, আপনি কীভাবে ইলেকট্রনের কোয়ান্টাম সংখ্যা খুঁজে পাবেন? কিভাবে কোয়ান্টাম সংখ্যার সাহায্যে ইলেকট্রনের সংখ্যা নির্ণয় করা যায়
- সম্পূর্ণ অরবিটাল গণনা করুন।
- প্রতিটি পূর্ণ অরবিটালের জন্য ইলেকট্রন যোগ করুন।
- কৌণিক কোয়ান্টাম সংখ্যা দ্বারা নির্দেশিত সাবশেল সনাক্ত করুন।
- সম্পূর্ণ সাবশেল থেকে ইলেকট্রন যোগ করুন।
- সম্পূর্ণ অরবিটাল থেকে পূর্ণ সাবশেল থেকে ইলেকট্রন যোগ করুন।
- চৌম্বকীয় কোয়ান্টাম সংখ্যার জন্য বৈধ ভ্যালস খুঁজুন।
এছাড়াও জানতে হবে, চারটি কোয়ান্টাম সংখ্যা কী কী?
পরমাণুতে, মোট চারটি কোয়ান্টাম সংখ্যা রয়েছে: প্রধান কোয়ান্টাম সংখ্যা (n), অরবিটাল কৌণিক ভরবেগ কোয়ান্টাম সংখ্যা (ঠ), দ চৌম্বকীয় কোয়ান্টাম সংখ্যা (মিl), এবং ইলেকট্রন স্পিন কোয়ান্টাম সংখ্যা (মিs).
একটি Subshell কি?
ক subshell ইলেকট্রন অরবিটাল দ্বারা বিভক্ত ইলেকট্রন শেলগুলির একটি উপবিভাগ। সাবশেলস একটি ইলেক্ট্রন কনফিগারেশনে s, p, d, এবং f লেবেলযুক্ত।
প্রস্তাবিত:
ত্রুটি নিরীক্ষণের জন্য কোন চারটি যন্ত্র ব্যবহার করা হয়?

চারটি যন্ত্র যা ত্রুটিগুলি নিরীক্ষণ করতে ব্যবহৃত হয় তা হল ক্রীপ মিটার, লেজার-রেঞ্জিং ডিভাইস, টিল্টমিটার এবং স্যাটেলাইট। একটি ক্রীপ মিটার মাটির পাশের গতিবিধি পরিমাপ করতে একটি ত্রুটি জুড়ে প্রসারিত একটি তার ব্যবহার করে। একটি লেজার-রেঞ্জিং ডিভাইস এমনকি সামান্য ত্রুটি আন্দোলন সনাক্ত করতে একটি প্রতিফলক থেকে বাউন্স করা একটি লেজার রশ্মি ব্যবহার করে
আন্তর্জাতিক একক ব্যবস্থায় সময়ের প্রমিত একক দ্বিতীয়টি কীভাবে সংজ্ঞায়িত করা হয়?

দ্বিতীয় (প্রতীক: s, সংক্ষিপ্ত রূপ: সেকেন্ড) হল ইন্টারন্যাশনাল সিস্টেম অফ ইউনিটস (SI) তে সময়ের ভিত্তি একক, যা সাধারণভাবে বোঝা যায় এবং ঐতিহাসিকভাবে একটি দিনের? 1⁄86400 হিসাবে সংজ্ঞায়িত - এই ফ্যাক্টরটি দিনের বিভাজন থেকে উদ্ভূত। প্রথমে 24 ঘন্টা, তারপর 60 মিনিট এবং অবশেষে 60 সেকেন্ড প্রতিটি
প্রাকৃতিক সংখ্যা পূর্ণ সংখ্যা পূর্ণসংখ্যা এবং মূলদ সংখ্যা কি?
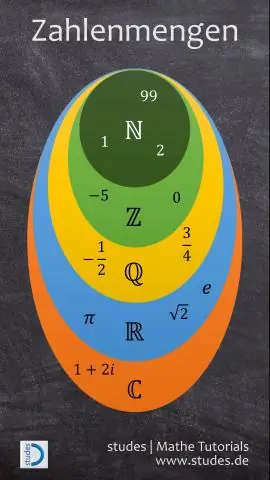
প্রকৃত সংখ্যাগুলি প্রধানত মূলদ এবং অমূলদ সংখ্যায় শ্রেণীবদ্ধ করা হয়। মূলদ সংখ্যা সব পূর্ণসংখ্যা এবং ভগ্নাংশ অন্তর্ভুক্ত. সমস্ত ঋণাত্মক পূর্ণসংখ্যা এবং পূর্ণ সংখ্যা পূর্ণসংখ্যার সেট তৈরি করে। পূর্ণ সংখ্যা সমস্ত প্রাকৃতিক সংখ্যা এবং শূন্য নিয়ে গঠিত
পূর্ণসংখ্যা এবং মূলদ সংখ্যা কী কী একটি স্থানাঙ্ক সমতলে বিন্দুগুলি কীভাবে গ্রাফ করা হয়?

আমরা যেমন বলেছি, স্থানাঙ্ক সমতলের বিন্দুগুলিকে (a, b) হিসাবে উপস্থাপন করা হয়, যেখানে a এবং b মূলদ সংখ্যা। মূলদ সংখ্যা হল এমন সংখ্যা যা ভগ্নাংশ হিসেবে লেখা যায়, p/q, যেখানে p এবং q হল পূর্ণসংখ্যা। আমরা বিন্দুর একটি x-স্থানাঙ্ক বলি এবং আমরা বিকে বিন্দুর y-স্থানাঙ্ক বলি
ভূতাত্ত্বিক টাইম স্কেলের উপবিভাগকে সংজ্ঞায়িত করতে এবং সনাক্ত করতে কীভাবে জীবাশ্ম ব্যবহার করা হয়েছে?

সূচকের জীবাশ্মগুলি ভূতাত্ত্বিক সময়ের আনুষ্ঠানিক স্থাপত্যে ব্যবহার করা হয় ভূতাত্ত্বিক সময়ের স্কেলের বয়স, যুগ, সময়কাল এবং যুগগুলি সংজ্ঞায়িত করার জন্য। এই ঘটনাগুলির প্রমাণ পাওয়া যায় জীবাশ্ম রেকর্ডে যেখানেই ভূতাত্ত্বিকভাবে স্বল্প সময়ের মধ্যে প্রজাতির প্রধান দলগুলির অন্তর্ধান হয়।
