
- লেখক Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:34.
- সর্বশেষ পরিবর্তিত 2025-06-01 05:03.
আরহেনিয়াস সমীকরণ : ln k = -Ea/R (1/T) + ln (A)<------ এটি হল y = mx + b ফর্ম সমীকরণ , তবে আমি কীভাবে এটি সমাধান করব তা বুঝতে সমস্যা হচ্ছে। ln k = - 0.0008313/8.314 J/mol কে (1/298 কে ) + ln (-0.8794) <---- এভাবেই আমি সংখ্যা সেট আপ করি কিন্তু আমি মনে করি না এটি সঠিক
এখানে, রসায়নে Ln K কী?
lnk = ln (Ae−Ea/RT)= ln A+ ln (e−Ea/RT) lnk = ln A+−EaRT=(−EaR)(1T)+ ln A. যা একটি সরলরেখার সমীকরণ যার ঢাল -Ea/R। এটি এর মান থেকে সক্রিয়করণ শক্তি নির্ধারণের একটি সহজ উপায় প্রদান করে k প্লট করে বিভিন্ন তাপমাত্রায় পর্যবেক্ষণ করা হয় lnk 1/T এর ফাংশন হিসাবে।
উপরন্তু, হার ধ্রুবক k কি? দ্য হার ধ্রুবক , k , একটি সমানুপাতিকতা ধ্রুবক যে reactants এবং মোলার ঘনত্ব মধ্যে সম্পর্ক নির্দেশ করে হার একটি রাসায়নিক বিক্রিয়া।
লোকেরা আরও জিজ্ঞাসা করে, সক্রিয়করণ শক্তির সূত্র কী?
অ্যাক্টিভেশন শক্তি নির্ধারণ. লক্ষ্য করুন যে যখন Arrhenius সমীকরণ উপরের মত পুনর্বিন্যাস করা হয় এটি y = mx + b ফর্ম সহ একটি রৈখিক সমীকরণ; y হল ln(k), x হল 1/T, এবং m হল -Eক/আর. বিক্রিয়ার জন্য সক্রিয়করণ শক্তি খুঁজে বের করে নির্ধারণ করা যেতে পারে ঢাল লাইনের
হার ধ্রুবক k জন্য একক কি?
দ্য ইউনিট এর k প্রতিক্রিয়া ক্রম উপর নির্ভর করে, কিন্তু ইউনিট প্রতি মিটারে কখনই নিউটন হয় না। একটি উদাহরণ হিসাবে, একটি প্রথম আদেশ প্রতিক্রিয়া জন্য, k আছে ইউনিট 1/s এবং একটি দ্বিতীয় অর্ডার প্রতিক্রিয়ার জন্য, ইউনিট 1/M.s.
প্রস্তাবিত:
আপনি কিভাবে PMP থেকে আদর্শ বিচ্যুতি গণনা করবেন?

আদর্শ বিচ্যুতির জন্য PMBOK-এ ব্যবহৃত সূত্রটি সহজ। এটা শুধু (P-O)/6। এটি হতাশাবাদী কার্যকলাপ অনুমান বিয়োগ আশাবাদী কার্যকলাপ অনুমান ছয় দ্বারা ভাগ। সমস্যা হল যে এটি কোন ভাবেই আকৃতি বা ফর্ম মানক বিচ্যুতির পরিমাপ তৈরি করে না
আপনি কিভাবে তার অক্ষাংশে পৃথিবীর পরিধি গণনা করবেন?

একটি বৃত্তের পরিধি 2πr এর সমান যেখানে r এর ব্যাসার্ধ। পৃথিবীতে, একটি প্রদত্ত অক্ষাংশে গোলকের পরিধি হল 2πr(cosθ) যেখানে θ অক্ষাংশ এবং r হল বিষুব রেখায় পৃথিবীর ব্যাসার্ধ
আপনি কিভাবে ফ্রিকোয়েন্সি এবং শতাংশ থেকে ফ্রিকোয়েন্সি গণনা করবেন?
এটি করার জন্য, ফলাফলের মোট সংখ্যা দ্বারা ফ্রিকোয়েন্সি ভাগ করুন এবং 100 দ্বারা গুণ করুন। এই ক্ষেত্রে, প্রথম সারির ফ্রিকোয়েন্সি 1 এবং ফলাফলের মোট সংখ্যা 10। শতাংশ তখন 10.0 হবে। চূড়ান্ত কলাম হল ক্রমবর্ধমান শতাংশ
আপনি কিভাবে একটি সার্কিটে সম্ভাব্য ড্রপ গণনা করবেন?
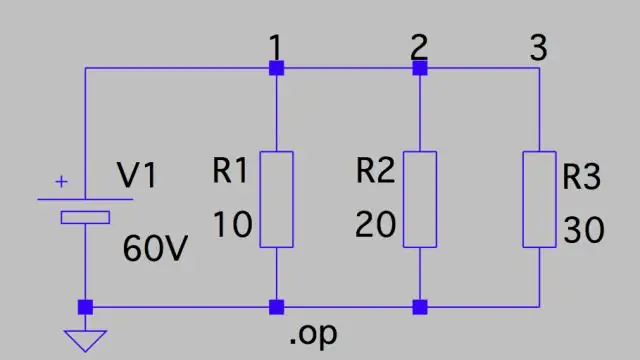
ভোল্টেজ ড্রপ: সমান্তরাল সার্কিট এর মানে হল যে প্রতিটি জুড়ে ভোল্টেজ ড্রপ সার্কিটের মোট ভোল্টেজকে সার্কিটের প্রতিরোধকের সংখ্যা দ্বারা ভাগ করা হয়, বা 24 V/3 = 8 V
আপনি কিভাবে ক্লোরিনের শতাংশ প্রাচুর্য গণনা করবেন?

18টি নিউট্রন সহ ক্লোরিন আইসোটোপের প্রাচুর্য রয়েছে 0.7577 এবং ভর সংখ্যা 35 amu। গড় পারমাণবিক ভর গণনা করতে, প্রতিটি আইসোটোপের ভর সংখ্যা দ্বারা ভগ্নাংশকে গুণ করুন, তারপরে তাদের একসাথে যোগ করুন
